ความแตกต่างระหว่าง EDTA และ EGTA
EDTA และ EGTA
EDTA และ EGTA เป็นสารก่อเจล ทั้งสองมีกรด polyamino carboxylic และมีสมบัติเหมือนกันมากหรือน้อย
EDTA
EDTA เป็นชื่อย่อของเอธิลีนไดเอไมน์ทราเฟอร์เอท เป็นที่รู้จักกันว่ากรด tetraacetic เอทิลีน (dinitrilo) tetraacetic ต่อไปนี้เป็นโครงสร้างของ EDTA
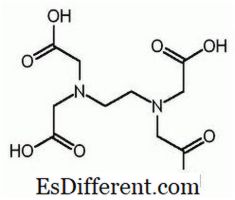
โมเลกุล EDTA มีหกตำแหน่งที่สามารถยึดโลหะไอออนได้ มีกลุ่มอะมิโนสองกลุ่มและกลุ่มคาร์บอกซิลสี่กลุ่ม อะตอมไนโตรเจนทั้งสองของกลุ่มอะมิโนมีคู่อิเล็กตรอนที่ไม่ได้แยกกันในแต่ละ EDTA เป็นแกนด์ hexadentate นอกจากนี้ยังเป็นตัวแทนจากคีเลตเนื่องจากความสามารถในการยึดโลหะไอออน EDTA ฟอร์ม chelates กับ cations ทั้งหมดยกเว้นโลหะอัลคาไลและ chelates เหล่านี้มีเสถียรภาพเพียงพอ ผลการทดสอบความมั่นคงจากบริเวณที่ซับซ้อนหลายแห่งในโมเลกุลที่ก่อให้เกิดโครงสร้างกรงคล้ายกับโครงสร้างรอบไอออนของโลหะ นี้แยกไอออนโลหะจากโมเลกุลของตัวทำละลายจึงป้องกัน solvation กลุ่มคาร์บอกซิลของ EDTA สามารถแยกโปรตอนที่บริจาคออกได้ EDTA มีคุณสมบัติเป็นกรด สายพันธุ์ EDTA ต่างๆมีคำย่อดังนี้ H 4 Y, H 3 Y - , H 2 Y 2-, HY3 - และ Y 4- ที่ pH ต่ำมาก (เป็นกลางที่เป็นกรด) รูปแบบ protonated ของ EDTA (H 4 Y) มีเด่นกว่า ในทางตรงกันข้ามที่ความเป็นกรด - ด่างสูง (ปานกลาง) รูป deprotonated อย่างเต็มที่ (Y 4- ) มีอิทธิพลเหนือกว่า และเมื่อค่าความเป็นกรด - ด่างเปลี่ยนจาก pH ต่ำไปเป็นค่าความเป็นกรด - ด่างสูงรูปแบบอื่น ๆ ของ EDTA จะมีอิทธิพลเหนือค่าพีเอชบางอย่าง EDTA สามารถใช้ได้ในรูปโปรตอนหรือแบบฟอร์มเกลือ Disodium EDTA และแคลเซียมดิโดเดรี EDTA เป็นรูปแบบเกลือที่ใช้กันมากที่สุด กรดอิสระ H 4 Y และ dihydrate ของเกลือโซเดียม Na 2 H 2 Y 2H 2 O มีจำหน่ายในเชิงคุณภาพ
คล้ายกับ EDTA EGTA ยังมีกลุ่มคาร์บอกซิลสี่กลุ่มซึ่งสามารถผลิตโปรตอนได้สี่ก้อนเมื่อแยกตัวออก มีอะมิโนสองกลุ่มและอะตอมไนโตรเจน 2 อะตอมของกลุ่มอะมิโนมีการแบ่งอิเล็กตรอนคู่กันในแต่ละกลุ่ม EGTA สามารถใช้เป็นบัฟเฟอร์คล้ายกับ pH ของเซลล์ที่มีชีวิต คุณสมบัตินี้ของ EGTA อนุญาตให้ใช้ในการทำ Tandem Affinity Purification ซึ่งเป็นเทคนิคการทำให้บริสุทธิ์ของโปรตีน
อะไรคือความแตกต่างระหว่างEDTA และ EGTA
?

• EDTA คือเอธิลีนไดเมทิลทราเฟอร์เอทและ EGTA เป็นเอธิลีนไกลคอล tetraacetic acid




